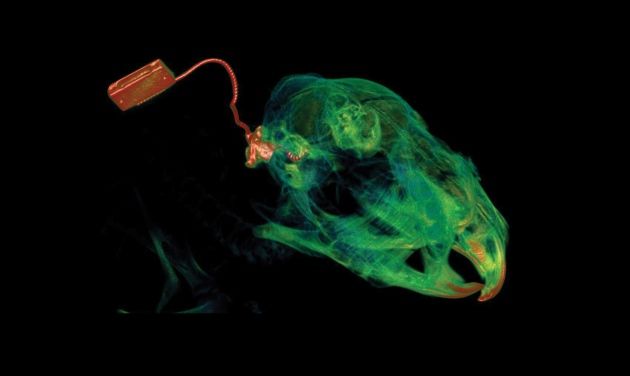
imagem de tomografia computadorizada que mostra o implante coclear no crânio de um porquinho-da-índia com deficiência auditiva. Crédito: unsw australia biological resources imaging laboratory e national imaging facility of australia
A terapia genética pode revolucionar o tratamento da perda de audição e aprimorar técnicas hoje empregadas pela medicina (como os implantes cocleares) para melhorar a vida dos portadores de sensibilidade auditiva reduzida.
Em dois estudos — um deles realizado por pesquisadores da Universidade de Nova Gales do Sul (UNSW), na Austrália; e outro, por uma equipe da Universidade do Kansas, nos Estados Unidos —, especialistas desenvolveram tecnologias capazes de reverter parte da perda auditiva através de diferentes métodos de terapia genética, que consiste na inserção de DNA terapêutico nas células de um paciente para substituir material genético danificado ou repará-lo. Inicialmente testada em animais, uma das novas técnicas deve estrear em experimentos com humanos em pouco tempo.
Afinação
No complexo fenômeno da audição, as ondas sonoras viajam até a orelha, fazendo com que o tímpano vibre; então, os ossículos do ouvido médio (estribo, bigorna e martelo) transferem a vibração ao órgão do ouvido interno, a cóclea, onde se localizam minúsculos receptores sensoriais conhecidos como células ciliadas. A vibração das células ciliadas, por sua vez, abre canais iônicos — poros moleculares pelos quais uma diferença de potencial elétrico permite o fluxo de íons — nas membranas das células do ouvido interno, ocasionando a passagem de neurotransmissores e, portanto, a conversão bioquímica da vibração do ar nos impulsos eletroquímicos que chegam ao cérebro.
Liderada pelo pesquisador Jeremy Pinyon, a equipe da UNSW enfocou uma das causas da perda de audição: a destruição de ligações celulares entre as células receptoras da cóclea e o nervo auditivo (que envia as informações ao cérebro). O implantes cocleares, por exemplo, utilizam eletrodos para estimular diretamente o nervo auditivo, transpondo o obstáculo imposto pela perda das conexões mencionadas. No entanto, no longo prazo, a perda de audição frequentemente faz com que as terminações nervosas atrofiem, tornando necessários para o paciente sinais elétricos mais fortes, a fim de que a conexão se complete, decorrendo disto a perda de resolução do som ouvido.
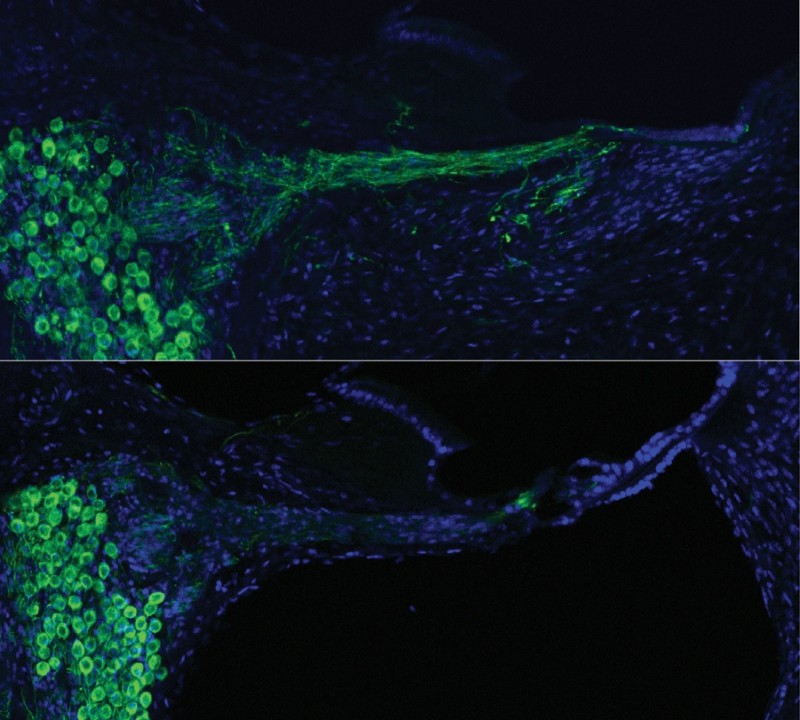
nervo coclear de um porquinho-da-índia reconstruído (acima e ao centro) a partir da terapia genética, em comparação com a situação pré-tratamento (abaixo). Crédito: unsw australia translational neuroscience facility, jeremy pinyon e gary housley
Para ajustar a “afinação” da audição auxiliada pelo implante coclear, os pesquisadores se aproveitaram dos impulsos elétricos enviados pelo dispositivo e da porosidade que eles provocam na membrana celular para inserir DNA saudável nas células auditivas de porquinhos-da-índia com surdez parcial, mais precisamente um gene que codifica a neurotrofina, classe de proteínas que promove o crescimento de nervos. Em estudo publicado no periódico Science Translational Medicine, a equipe relata que, após a injeção genética e uma série de impulsos elétricos, as células passaram a produzir a neurotrofina, e o nervo auditivo, a se regenerar (imagem acima), chegando novamente à cóclea e aprimorando o aproveitamento sensorial dos impulsos transmitidos pelo implante.
O uso da tecnologia para a obtenção de sons legitimamente mais naturais ainda requer uma evolução nos implantes cocleares e experimentos clínicos com humanos estão distantes, mas “[a abordagem] é a mais promissora até hoje”, de acordo com Gerald Loeb, pesquisador da University of Southern California e desenvolvedor do implante original.
Vírus, ao trabalho!
Como já dito, pacientes com nervos auditivos mais danificados necessitam sinais elétricos muito potentes, o que acaba por dificultar o reconhecimento das diferentes frequências sonoras, prejudicando, por exemplo, a identificação de vozes e a apreciação da música. “O santo graal é devolver às pessoas a audição natural”, diz Hinrich Staecker, do Centro Médico da Universidade do Kansas, que deve iniciar experimentos com voluntários humanos no próximo mês. O objetivo de Staecker e seus pares é “reparar o ouvido, ao invés de imitar artificialmente o que ele faz”.

células ciliadas plenamente funcionais no ouvido interno. Crédito: steve gschmeissner/spl
Os holofotes dos pesquisadores do Kansas se voltaram para a perda das células ciliadas da cóclea, que pode se dar devido a ruídos de amplitude excessiva, doenças e consumo de determinadas drogas. Em 2003, cientistas descobriram genes capazes de transformar em células ciliadas as células que dão suporte às ciliadas, e um desses genes — denominado Atoh1 — foi testado por Staecker em camundongos.
Realizada no ano passado, a pesquisa consistiu na introdução do gene em um vírus inofensivo. Este, por sua vez, foi inserido na cóclea de camundongos que haviam perdido quase todas as suas células ciliadas. Dois meses depois, a capacidade auditiva dos roedores tinha melhorado em cerca de 20 decibéis, a mesma diferença entre “ouvir com suas mãos sobre os ouvidos e o que você ouve habitualmente”, conforme Lloyd Klickstein, membro da Novartis, empresa farmacêutica que colaborou no experimento. Além disso, verificou-se que o vírus não se espalhou pelos demais tecidos do corpo, mantendo-se no local da injeção.
Agora, a equipe espera conseguir voluntários (com idades entre 18 e 70 anos) portadores de perda auditiva crônica ocasionada pela destruição das células ciliadas. Os voluntários terão o vírus portador do gene Atoh1 injetado diretamente nas cócleas e, da mesma forma como no caso dos roedores, espera-se que o objetivo seja atingido em um período que vai das duas semanas aos dois meses seguidos à intervenção.
 Make It Clear Brasil
Make It Clear Brasil
Um apoio ao livre pensamento e a um entendimento do mundo baseado em evidências
 Make It Clear Brasil
Make It Clear Brasil








Comentários